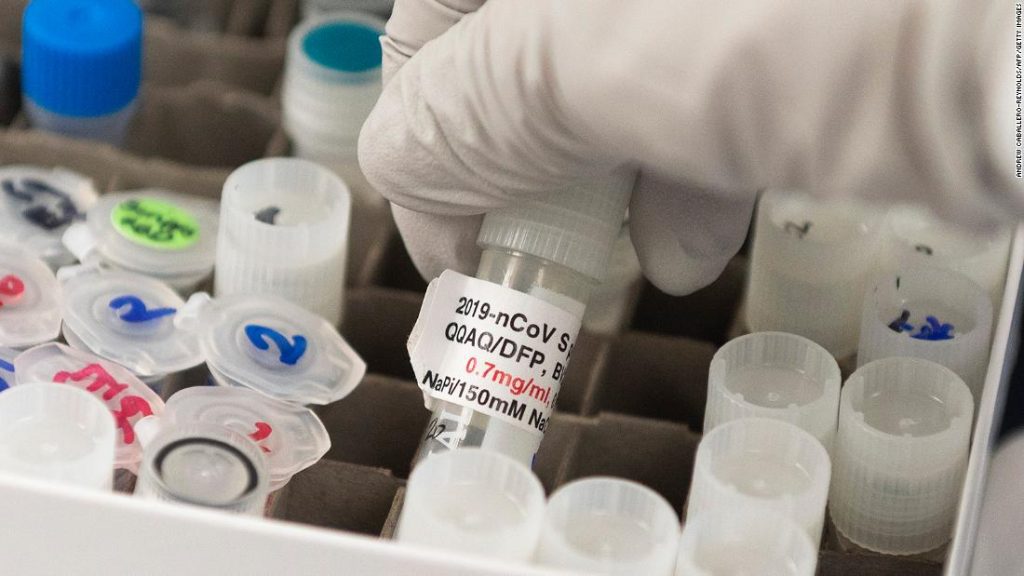
Sebagian besar Komite Penasihat FDA tentang Vaksin dan Produk Biologi Terkait memilih “ya” sebagai jawaban atas pertanyaan tentang apakah manfaat vaksin Novavax, yang diberikan sebagai seri awal dua dosis, lebih besar daripada risikonya pada orang berusia 18 tahun atau lebih. , berdasarkan bukti yang tersedia . Dua puluh satu anggota memilih ya, satu abstain, dan tidak ada yang memilih “tidak”.
Jika Food and Drug Administration (FDA) memberi lampu hijau pada vaksin, itu akan menjadi vaksin Covid-19 keempat yang dilisensikan di Amerika Serikat.
Vaksin Novavax dibuat menggunakan potongan-potongan kecil yang dibuat di laboratorium virus corona untuk merangsang kekebalan. Pendekatan berbasis protein ini merupakan pendekatan yang lebih tradisional untuk pengembangan vaksin daripada vaksin mRNA dari Pfizer/BioNTech dan Moderna.
Anggota komite Dr. Jay Portnoy, profesor pediatri di Fakultas Kedokteran Universitas Missouri-Kansas City, mengatakan dia melihat pemungutan suara sebagai peluang.
“Ini adalah teknologi yang berbeda. Ini adalah vaksin berbasis protein yang lebih tradisional,” kata Portnoy. “Vaksin layak mendapat kesempatan untuk diberikan dan dipelajari.”
“Tentu saja, manfaatnya lebih besar daripada risiko dari rangkaian awal,” kata anggota panel Dr. Michael Nelson, ketua divisi Asma, Alergi, dan Imunologi Klinis di Fakultas Kedokteran Universitas Virginia, tentang pemungutan suara tersebut.
“Saya pikir kelompok ini sangat sadar bahwa ini kemungkinan merupakan rangkaian tiga dosis, dan kemudian Anda perlu mengumpulkan data yang mendukung perlunya dosis booster dan dosis pasca-dosis untuk menjadikannya mungkin vaksin tiga dosis,” katanya, mengisyaratkan bagaimana diskusi dapat dilanjutkan untuk menggunakan vaksin sebagai suntikan pendorong.
Kasusnya mirip dengan miokarditis setelah vaksin mRNA Covid-19 yang dikembangkan oleh Pfizer/BioNTech dan Moderna, dan mereka meningkatkan “kekhawatiran tentang hubungan sebab akibat” dengan vaksin Novavax, menurut dokumen FDA.
Novavax mencari otorisasi AS
Pada bulan November, Indonesia menjadi negara pertama yang memberikan otorisasi penggunaan darurat untuk vaksin Novavax. Ini juga dilisensikan di Uni Eropa, Inggris, Kanada, Korea Selatan, Australia, India, Filipina, dan Selandia Baru, di antara negara-negara lain.
Novavax siap mengirimkan dosis vaksinnya dari Serum Institute of India ketika disahkan oleh Food and Drug Administration.
“Kami berharap FDA akan mengambil rekomendasi panel VRBPAC ini … bersama dengan semua data manufaktur yang kami berikan kepada mereka dan hasil pemeriksaan mereka terhadap pabrik kami di India, dan dapat mengambil keputusan. Kami berharap ini segera,” kata Stanley Erk , presiden perusahaan Novavax dan CEO-nya, mengatakan kepada CNN pada hari Selasa.
Dia mengatakan pengiriman pertama perusahaan ke Amerika Serikat akan menjadi “beberapa juta” dosis.
Adapun siapa yang dapat menerima vaksin, Erk mengatakan, “Ada puluhan juta orang yang belum menerima vaksin utama mereka karena satu dan lain alasan.” “Ini adalah salah satu pasar bagi kami.”
Dia menambahkan bahwa pasar lain untuk vaksin termasuk anak-anak dan, pada akhirnya, orang-orang yang membutuhkan dosis booster untuk mempertahankan perlindungan terhadap Covid-19.
Permintaan izin Novavax didasarkan pada data termasuk hasil dari dua uji klinis besar yang menunjukkan kemanjuran keseluruhan sekitar 90% dan “profil keamanan yang meyakinkan,” menurut perusahaan. Uji coba dilakukan sebelum varian virus corona Omicron mendominasi di Amerika Serikat.
“Rekomendasi positif komite penasihat mengakui kekuatan data kami dan pentingnya vaksin COVID-19 berbasis protein yang dikembangkan menggunakan pendekatan inovatif terhadap teknologi vaksin konvensional,” kata Erk dalam sebuah pernyataan setelah pertemuan Selasa.
“Pada pertemuan VRBPAC hari ini, kami mendengar dukungan besar untuk vaksin dari dokter, organisasi kesehatan, dan konsumen yang sangat menantikan pilihan vaksin berbasis protein,” katanya. “Kami menantikan keputusan FDA.”
Secara umum, penyerapan vaksin Covid-19 – terutama dosis booster – di AS lambat, dan seorang pejabat Administrasi Makanan dan Obat-obatan menggambarkannya sebagai masalah “sangat serius” pada pertemuan hari Selasa.
“Kami memiliki masalah yang sangat serius dengan vaksin di Amerika Serikat, dan apa pun yang dapat kami lakukan untuk membuat orang lebih nyaman menerima produk obat yang menyelamatkan jiwa ini adalah sesuatu yang kami rasa harus kami lakukan,” kata Dr. Peter Marks, direktur Pusat Evaluasi dan Penelitian Biologi.
Eric Rubin, pemimpin redaksi New England Journal of Medicine dan anggota VRBPAC, bertanya pada pertemuan tersebut mengapa vaksin Covid-19 lain diperlukan di AS ketika tiga diotorisasi atau disetujui: vaksin dari Pfizer/BioNTech, Moderna, dan Jansen dari Johnson & Johnson.
“Vaksin Janssen saat ini tidak digunakan sebagai vaksin garis depan dengan cara yang sama seperti vaksin mRNA, meninggalkan pertanyaan tentang vaksin kepada mereka yang mungkin tidak ingin mengambil vaksin mRNA karena kekhawatiran yang mungkin mereka miliki,” jawab Marks, merujuk pada vaksin yang dikembangkan. oleh Pfizer/BioNTech dan Moderna. .
“Memiliki alternatif berbasis protein mungkin lebih nyaman bagi sebagian orang dalam hal penerimaan mereka terhadap vaksin,” kata Marks.
Vaksin berbasis protein seperti Novavax bekerja dengan membuat sistem kekebalan tubuh mengenali potongan kecil virus yang mereka targetkan. Dalam hal ini, itu berarti pemotongan dari protein lonjakan virus corona.
Ilmuwan Novavax telah mengidentifikasi gen untuk protein lonjakan dan menciptakan versi modifikasi dari gen ini. Para peneliti mengkloning gen dalam baculovirus yang menginfeksi serangga. Mereka kemudian menginfeksi sel ngengat – khususnya, sel-sel dari Fall Armyworm – yang mendorong mereka untuk menghasilkan protein lonjakan virus corona. Nanopartikel mirip virus ini dipanen untuk membuat vaksin Novavax.
Secara keseluruhan, vaksin bergantung pada teknologi nanopartikel rekombinan dan adjuvant Novavax, yang disebut Matrix-M, untuk merangsang respons imun dan antibodi penetralisir tingkat tinggi.
“Itu tidak menular. Kami tidak pernah menyentuh virus corona itu sendiri.” “Dan kemudian itu diberikan kepada orang-orang, dan mereka melakukan respons imun yang sangat terfokus hanya pada lonjakan — dan saya akan mengatakan, ciri khas vaksin kami adalah memberikan respons imun yang sangat kuat dengan sedikit efek samping, dosis sangat kecil dan vaksin dapat disimpan pada suhu normal. didinginkan.”

“Geek tv yang sangat menawan. Penjelajah. Penggemar makanan. Penggemar budaya pop yang ramah hipster. Guru zombie seumur hidup.”




/cdn.vox-cdn.com/uploads/chorus_asset/file/24931352/236792_iPhone_15_Pro_and_15_Pro_Max_product_photos_AJohnson_0008.jpg)
More Stories
Kanada mengenakan tarif 100% pada impor mobil listrik Tiongkok
JPMorgan memperkirakan The Fed akan menurunkan suku bunga acuannya sebesar 100 basis poin tahun ini
Foot Locker meninggalkan New York dan pindah ke St. Petersburg, Florida untuk mengurangi biaya tinggi: “efisiensi”